Estamos terminando mais uma semana e para vocês mais um blog post pedagógico, dessa vez sobre Termodinâmica, a área da física (confira nesse link algumas dicas de como estudar física para o Enem) que estuda a transferência de energia, ou seja, estudo das leis que regem as relações entre calor, trabalho e outras formas de energia.
Só aluno Explicaê Premium tem correções ilimitadas das suas redações.
Antes de tudo, vocês sabem como começou o estudo da Termodinâmica? Então, durante a Revolução Industrial, com uso das máquinas, várias ferramentas e utensílios, bem como algumas tarefas antes exercidas pelos operários tornaram-se obsoletas.
Dentre as máquinas, na época, ganham destaque as máquinas térmicas sendo as mais utilizadas. Esse tipo de máquina tem seu funcionamento baseado na transformação da energia térmica (calor) em energia mecânica (trabalho).
Atualmente a indústria e setor de transporte vem se beneficiando do crescente “know how” adquirido pelo desenvolvimento da termodinâmica.
Um grande avanço nos meios de transportes, como o barco a vapor e a locomotiva a vapor, e no setor de produção em massa impulsionou a criação de máquinas cada vez mais eficientes e seguras.
Nesse cenário ganha destaque o inventor escocês James Watt pelos melhoramentos que introduziu no motor a vapor, que se constituíram num passo fundamental para transição que ocorria com a grande revolução.
A máquina a vapor de Watt passou a ser amplamente usada nas fábricas, sendo consideradas um dos fatores que provocaram a famosa Revolução Industrial.
TRABALHO TERMODINÂMICO
Quando confinamos um gás em um recipiente dotado de um embolo móvel, podemos obter desse sistema uma quantidade de trabalho.
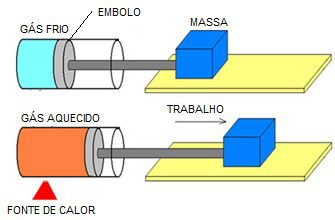
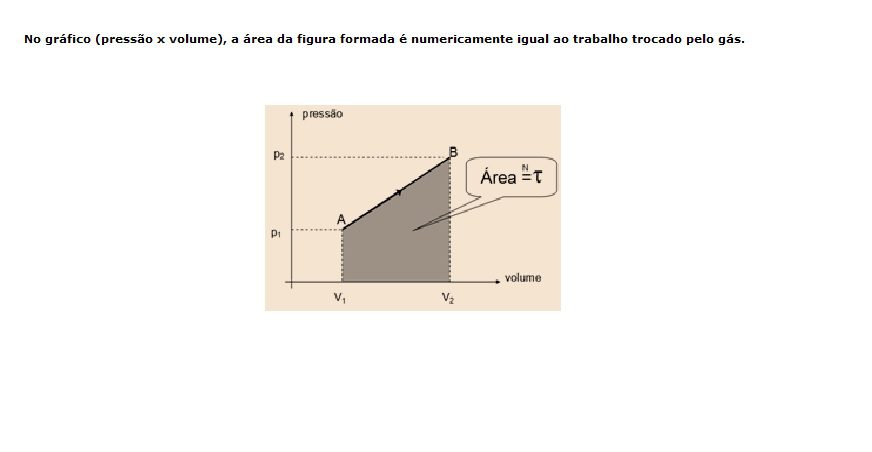
Determinamos o trabalho de um gás, conhecendo-se a sua pressão e a variação do volume que o gás sofre pela expressão:

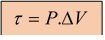
Exercícios Resolvidos
1. (ENEM 2014) Um sistema de pistão contendo um gás é mostrado na figura. Sobre a extremidade superior do êmbolo, que pode movimentar-se livremente sem atrito, encontra-se um objeto. Através de uma chapa de aquecimento é possível fornecer calor ao gás e, com auxílio de um manômetro, medir sua pressão.
Só aluno Explicaê Premium tem acesso a dúvidas ilimitadas.
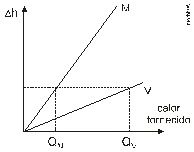
A partir de diferentes valores de calor fornecido, considerando o sistema como hermético, o objeto elevou-se em valores como mostrado no gráfico. Foram estudadas, separadamente, quantidades equimolares de dois diferentes gases, denominados M e V.

A diferença no comportamento dos gases no experimento decorre do fato de o gás M, em relação ao V, apresentar
a) maior pressão de vapor.
b) menor massa molecular.
c) maior compressibilidade.
d) menor energia de ativação.
e) menor capacidade calorífica.
RESOLUÇÃO
Como mostrado no gráfico, para uma mesma elevação a quantidade calor absorvido pelo gás é menor do que a absorvida pelo gás.
Mas, para uma mesma variação temos também uma mesma variação de volume Como se trata de transformações isobáricas, os trabalhos realizados também são iguais.
Supondo gases ideais:
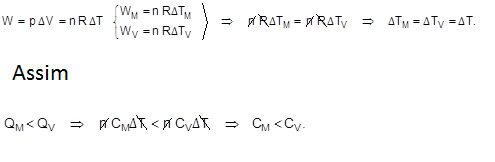
RESPOSTA: LETRA E
2. (ENEM 2015) O ar atmosférico pode ser utilizado para armazenar o excedente de energia gerada no sistema elétrico, diminuindo seu desperdício, por meio do seguinte processo: água e gás carbônico são inicialmente removidos do ar atmosférico e a massa de ar restante é resfriada até Presente na proporção de dessa massa de ar, o nitrogênio gasoso é liquefeito, ocupando um volume vezes menor.
A energia excedente do sistema elétrico é utilizada nesse processo, sendo parcialmente recuperada quando o nitrogênio líquido, exposto à temperatura ambiente, entra em ebulição e se expande, fazendo girar turbinas que convertem energia mecânica em energia elétrica.
MACHADO, R. Disponível em www.correiobraziliense.com.br Acesso em: 9 set. 2013 (adaptado).
No processo descrito, o excedente de energia elétrica é armazenado pela:
a) expansão do nitrogênio durante a ebulição.
b) absorção de calor pelo nitrogênio durante a ebulição.
c) realização de trabalho sobre o nitrogênio durante a liquefação.
d) retirada de água e gás carbônico da atmosfera antes do resfriamento.
e) liberação de calor do nitrogênio para a vizinhança durante a liquefação.
RESOLUÇÃO
Ao interpretar o texto, é possível perceber que o nitrogênio é o responsável pela geração de energia. Ele apresenta um estado inicial; depois, ele “é liquefeito, ocupando um volume 700 vezes menor”, para, em seguida, expandir ao estado inicial, quando é utilizado para girar as turbinas.
Só aluno Explicaê Premium tem acesso ao conteúdo completo e ilimitado.
O armazenamento da energia ocorre na segunda etapa, quando ele é liquefeito.
RESPOSTA: LETRA C
E aí, o que achou do blog? Comenta aqui embaixo outros assuntos que você gostaria de ver por aqui 🙂
Só aluno Explicaê Premium tem acesso ilimitado a mais de 6.000 livros em PDF.
