Olá, vestibulande! Abordaremos neste blog a reação química chamada de oxirredução. Falar dessa reação é como falar da própria existência. A vida depende diretamente dessa reação. Você já percebeu o quanto esse assunto é importante, né? Então só vem, bb. Vamos juntos aprender! hehe
Só aluno Explicaê Premium tem acesso as provas e gabaritos de vestibulares de todo o Brasil.
Então, chuchu, exemplos clássicos de oxirredução é a fotossíntese e a respiração celular. A respiração celular é a oxidação dos carbonos da glicose, enquanto a fotossíntese é a redução de carbonos do gás carbônico transformando-os em glicose.

Se você pensar que a fotossíntese produz moléculas de glicose para que elas possam ser utilizadas pelos seres vivos para produzir energia para a sua sobrevivência, a gente pode dizer, sem medo de errar, que essa reação é, no mínimo, perfeita.

A oxirredução também tem o seu lado ruim do ponto de vista de ser humano e isso não posso deixar de mostrar, veja que, quando colocamos um portão de ferro em casa e depois de um certo tempo vejo-o sofrendo corrosão, então fico enraivado com a oxirredução, a responsável por causar esse estrago no meu portão.

Uma outra situação bastante triste é a o ataque dos radicais livres ao nosso material genético causando mutações gênicas e levando a célula a uma condição de inutilidade denominada de câncer.

A oxirredução é um casamento indissociável de duas reações, em que uma já mais existe sem a outra, a oxidação e a redução. Mas o que caracteriza uma oxidação e uma redução? A oxidação é a reação de perda de elétrons por parte de um material, enquanto a redução é o ganho desses elétrons por um outro material, veja que uma não pode viver sem a outra, pois, para um material perder elétrons, é necessário que o outro esteja apto a receber esses elétrons.
Dessa forma, quando uma espécie química perde elétrons, podemos entender que ela acaba obrigando a outra a sofrer redução. Por isso podemos dizer que quem oxida é o causador da redução do outro e, por esse motivo, é chamado de agente redutor ou simplesmente redutor e, dessa mesma forma, podemos analisar a redução. Quando um material reduz, ele provoca a oxidação do outro material e, desse modo, é chamado de agente oxidante ou simplesmente oxidante.
Aí vem uma pergunta: como saber se uma espécie química oxidou ou reduziu? Dessa forma que entra em cena o tal do NOX, conhecido como número de oxidação, uma carga que demonstra se a espécie perdeu ou ganhou elétrons, vejamos um exemplo: a espécie Na+ apresenta uma carga 1+, o que significa que ela perdeu elétrons e, por isso, podemos dizer que ela sofreu oxidação, e assim podemos dizer que o Na+ está oxidado, um outro exemplo é O2-, que representa que o oxigênio ganhou 2 elétrons ou seja sofreu redução e por isso podemos dizer a espécie encontra-se reduzida.
Então é dessa forma, através do NOX, que podemos afirmar qual espécie oxidou e qual reduziu. Agora vejamos um exemplo aplicado em uma reação:
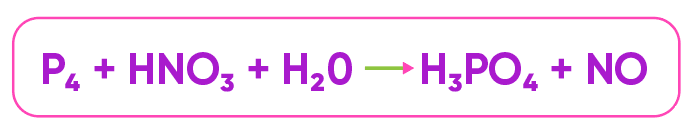
No P4 o nox P é zero e no H3PO4 o nox do P é +5, então de 0 até +5 podemos afirmar que o P sofreu oxidação (crescimento do nox), e assim O H3PO4 é considerado um agente redutor ou simplesmente redutor.
No HNO3 o nox do N é +5 e no NO o nox do N é +2, então de +5 para +2 houve um ganho de elétrons que gerou uma redução do nox do N, assim podemos afirmar que o N sofreu redução e o HNO3 é o agente oxidante ou simplesmente oxidante.
Mas não para por aí, uma oxirredução tem várias aplicações e o homem resolveu usar essa reação ao seu favor para trazer uma melhoria nas condições de vida da humanidade e, assim, criou, por exemplo, a pilha, um exemplo de oxirredução espontânea capaz de gerar corrente elétrica, que faz funcionar inúmeros aparelhos como os celulares e o marca-passo que garante a vida daqueles que tiveram o coração infartado.
Sabe aquela coisa da oxidação provocar a corrosão de uma estrutura metálica importante para nós seres humanos? Achamos uma solução para isso, resolvemos colocar um metal de alta capacidade de oxidação (alto potencial de oxidação) para proteger um outro metal e evitar, dessa forma, a corrosão do metal que me interessa em razão da oxidação de um outro metal, estou falando do metal de sacrifício.
Só aluno Explicaê Premium tem acesso ao conteúdo completo e ilimitado.
Vejamos o exemplo disso: a fim de proteger o ferro que possui o potencial de oxidação + 0,44V, ligamos a esse metal um pedaço de magnésio que possui um potencial de oxidação + 2,37V, e dessa forma podemos afirmar que o magnésio sofre oxidação impedindo a oxidação do ferro, e assim classificamos o magnésio como metal de sacrifício.
Pois é, pessoal. Devemos respeitar e entender a reação de oxirredução. Além disso, devido à sua importância para a humanidade, acredito que sempre será motivo de questões nos exames, viu, bb? Por isso, estudem essa reação que a probabilidade de estar nas provas é muito grande.
